Introducción
Antes de comenzar la discusión
especifica sobre el procedimiento de trasplantación, debemos revisar
brevemente el potencial terapeuticote de varias células y tejidos que han
sido incorporadas en la trasplantación celular, programa diseñado para
restaurar algunas funciones después de lecciones de la columna vertebral.
Tejido de la Olfatoria/ Células:
Porque el tejido de la olfato esta expuesto al
aire que respiramos, este contiene células de alto nivel de rotación,
incluyendo la renovación de neuronas, célula madre urogenital y células
olfativas de ensheathing (OECs). ]
Cuando trasplantación es aplicada en
área dañada de la columna vertebral, potencial de regeneración del axon
puede existir, produciendo myelin sheaths alrededor del tejido dañado y
del tejido en crecimiento, segregando factores de crecimiento que generan
macromoléculas de matriz y estructura funcional, dejando las huellas para
la elongación del axon.
Stem Cells (Célula Madre):
Brevemente, las células madre son precursoras o
células progenitales que tienen el potencial de transformarse en cierta
variedad de tejidos. Aunque estas han sido categorisadas como embronicas o
adultas, en realidad estas representan la continuidad de un tipo de
células, la cual se puede transformar en un nuevo tejido especifico.
Por ejemplo, mediante el desarrollo
de nuestro sistema nervioso central (SNC), las células madre embrionicas
se evolucionan en células madre adulta, neurológica especializadas. En
cambio, estas células adultas se pueden diferencial en neuronas o en
glial-precursoras restringidas, formadoras con potencial de transformarse
en neuronas y después en células que apoyan a las oligodendrocytes y
astrositos.
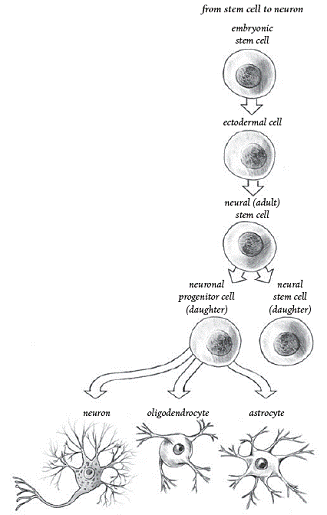
Células madre embrionicas
omnipotentes tienen la mayor potencial de diferenciarse entre una amplia
variedad de células, su manejo hacia la dirección deseada a sido
dificultoso. Células madres adultas han sido encontrada en casi todos los
tejidos, incluyendo los tejidos nervioso central, de medula ósea, de piel,
de intestino, de hígado, muscular, de cabello y hasta de los dientes.
Algunas veces estas células son fuertemente expresadas de tal manera que
la medula ósea produce células madre en cantidades mas que suficiente; en
otros tejidos estas se encuentran dormanes que se pueden altivar.
Aunque las células madres adultas
usualmente se diferencian en células especializadas conectadas con el
tejido de oringe y
algunas claves son proveídas, estas células se pueden transformar en
células asociadas con otros tejidos. Por ejemplo, bajo la circunstancia
apropiada, la célula ósea derivada de la estigma se puede diferencial en
una neurona, ciertamente han sido usadas en muchas de las lesiones de la
medula espinal. Para añadir, lose estudios sugieren que las células madres
adultas pueden ser reprogramadas en un estado mas embrionoco. Finalmente,
aunque hemos enfatizado su potencial terapéutico, estas se pueden
convertir en una amenaza fisiológica, un ejemplo es la causa de cáncer.
Aislamiento embrionario de la
Célula Madre: Básicamente, después de que un
huevo sea fertilizado, un embrión es formado, cual parte en un embrión
de dos-células. En Stem Cell Now, el autor Cristóbal Scott
compara el proceso de dividir una burbuja del jabón con un cuchillo,
creando dos burbujas más pequeñas dentro de los límites de la original.
Otro corte, y llega a ser cuatro burbujas o un embrión de
cuatro-células. Esta división pasa, creando sucesivamente 8, 16, 32, 64,
embriones de 128 células, el volumen total que cambia poco.
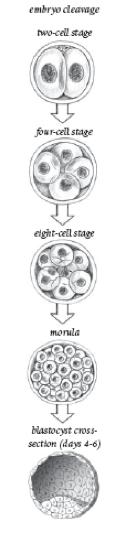
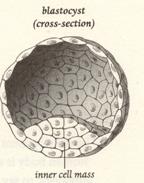
Entre cuatro y seis días, las
células se arreglan en dos capas: una capa exterior que se convertirá en
los tejidos que forman la placenta y líquido amniótico y otras pocas
docenas de células llamadas la masa interior-celular (ICM) que se
convierten en lo de más. Ahora marcado blastocyst, el embrión está
acerca de 0.1-mm a través o de tamaño del período a fines de esta
oración.
Medientras las células continúan su
desarrollo, ellas pierden cada vez más su naturaleza omnipotente.
Después acerca de dos semanas, las células de ICM empiezan a organizar
se en tres capas específicas que llegan a ser nuestros varios tejidos:
1) capa ectodérmica (convirtiéndose en el nervio, la piel, etc.), 2)
mesodérmica (volviéndose en la sangre, el músculo, el hueso, etc.), y 3)
endodérmica (diferenciando se en el intestino, el hígado, el páncreas,
la vejiga, etc.).
Para obtener ESC, las células
de ICM son aisladas antes de convertirse en estas capas, y se crecen en
cultura. La tecnología que cultiva sólo ha surgido recientemente y
requiere la metodología y la habilidad sofisticada. Por ejemplo, los
científicos han tenido que crecer las células en una capa de células
animales para proporcionar alimentos nutritivos y las señales necesarias
para detener las células de diferenciación adicionar.
Células de Shwann Estas
células son responsables por envainar el axons en el sistema nervioso
periférico, que, a diferencia del SNC, tiene el potencial regenerador,
inherente y considerable. Ha habido con el paso de los años mucha
especulación en el potencial de estas células de ejercer los efectos
semejantes y regeneradores cuando son introducidas en lesiones de la
medula espinal.
Fuente Celular & Sitio de
Transplante: Las células transplantables pueden
ser obtenidas del paciente (autologous); individuos genéticamente
diferentes, de embriones, o de cordones umbilicales (allogeneic); o de una
especie diferente (xenogeneic). Los tres tipos han sido trasplantados en
un esfuerzo de restaurar la función después de SCI (lesión de la medula
espinal). Porque el tejido autologous es del paciente, no hay rechazo
inmunológico. La naturaleza indiferenciada del embrionario y, a un grado
menor, las células umbilicales aminoran también el rechazo.
Las células del donante son
trasplantadas en el paciente por una variedad de rutas, incluyendo en la
médula espinal o en líquido, intravenosa mente, o intramuscularmente. En
general, las células no son escogidas basado en la mejor fuente teórica ni
el potencial regenerador pero por la comodidad del aislamiento, como
concentrando las células madre de sangre; e, igualmente, es mucho más
fácil (y más seguro pero quizás no como efectivo) inyectar las células en
un músculo, en la sangre, o en el líquido espinal que intervenir
quirúrgicamente a la médula espinal.
Por ejemplo, científicos
checos desarrollan procedimientos que utilizan imagines de resonancia
magnética (IRM). Básicamente, con estos procedimientos, partículas
magnéticas muy pequeñas de óxido de hierro están conectadas a las
células madre, haciendo las visibles por IRM, y en cambio, esto permite
seguir las hasta cierto punto después del trasplante. El objetivo
general de la investigación es de determinar el curso de tiempo de
migración al sitio lesionado y cuánto tiempo las células persisten allí.
Con tal información, nosotros podemos comprender mejor la agenda óptima
para el trasplante, el número de células necesitadas, y de la mejor ruta
de la administración.
En otro ejemplo, un equipo
internacional de científicos ha utilizado procedimientos de imaginen
magnética para valorar la migración de células olfativas marcadas por el
óxido de hierro que han sido trasplantadas en la médula espinal en ratas.
Las OECs marcadas pudieron ser observadas en la médula espinal por lo
menos dos meses después del trasplante. Aunque la migración extensa de
OECs trasplantadas fuera observada en una y otra dirección en la
médula espinal normal, las células no pudieron emigrar por la
cicatriz del sitio lesionado en la médula espinal transversalmente
cortada.
Edad & Nivel de Lesión:
Otros factores que pueden influir la
eficacia terapéutica de las células madre incluyen la edad y el nivel de
lesión. Como mostrado por investigadores del RU, esto parece ser el caso
para células madre de médula ósea, que han sido trasplantada en varios
programas relacionado con SCI. En este estudio, la médula ósea fue
aislada de la cresta ilíaca (es decir, un área del pelvis) de donantes
con SCI y crecidas en cultura. La edad del donante recorrió de 23-66
años, y todos tuvieron lesiones completas sostenidas cinco meses a 23
años antes que el tejido de médula ósea fuera reunido. Aunque la
cantidad de la muestra fuese limitada, el crecimiento de las células
madre en la cultura fue mayor cuando las células fueron aisladas de
pacientes más jóvenes y de ésos con lesiones cervicales.
El Dr. Carlos Lima, quien
desarrolló procedimientos para trasplantar células madre contiendo
tejido olfativo en la cuerda lesionada, no aceptará a pacientes mayores
de 40 debido a la disminución de potencia regeneradora en este tejido
con la edad.
TOP