
1)
4-Aminopyridine
2) HP-184
3)
Theophylline
4) Lithium
5) Fibroblast Growth Factor

ФАРМАЦЕВТИЧЕСКИЕ МЕТОДЫ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ТСМ
1)
4-Aminopyridine (4AP or Fampridine-SR)
1)
4-аминопиридин (4AP или фампридин-SR)
4AP –
маленькая молекула, восстанавливающая некоторые функции у некоторых
людей с ТСМ. Она улучшает проводимость неповрежденных, но
демиелинизированных нейронов, которые зачастую сохраняются в области
травмы, не только при неполном повреждении, но и при повреждении,
клинически классифицируемом как полное. Согласно оценкам, 4AP
может принести пользу примерно трети пациентам с ТСМ.
Поскольку демиелинизированные
нейроны потеряли свою изолирующую оболочку, они больше не могут
передавать сигналы. Без изолирующего миелина, каналы между наружной и
внутренней сторонами аксонов обнажаются. Из-за этого воздействия ионы
калия истекают из аксона, в свою очередь, замыкая трансмиссию нейронов.
Блокируя эти каналы, 4AP способствует проведению
сигналов через демиелинизированные области.
Поскольку в механизме действия 4AP
участвуют демиелинизированные нейроны, вещество было впервые
протестировано на пациентах с рассеянным склерозом (РС). И ТСМ и РС
являются заболеваниями, для которых характерна потеря изолирующего
миелина вокруг нейронов; при РС это вызвано аутоимунными причинами,
тогда как при ТСМ потеря миелина вызвана травмой.
4AP не
стимулирует регенерацию и не способствует улучшению физиологии или
биологии после травмы, соответственно, не является средством излечения,
а лишь временно усиливает существующие функции, т.е. представляет собой
средство временного воздействия.
Когда организм избавляется от 4AP,
полезный эффект от него теряется. Состав с замедленным высвобождением 4AP
достигает максимальной концентрации в крови примерно через 2-3 часа
после введения, и период полувыведения составляет приблизительно 6-7
часов. Согласно исследованиям, оценивающим выведение принимаемого
перорально 4АР, помеченного радиоактивными маркерами, препарат
отсутствует в организме почти полностью через 24 часа (3). Для
поддержания нужного уровня 4AP в крови необходимо
постоянно принимать 4AP несколько раз в день.
Другими словами, любая восстановленная функция исчезнет, если прекратить
прием препарата.
Обзор вебсайтов, посвященных ТСМ,
свидетельствует о том, что многие пациенты с ТСМ принимали 4AP,
в составе препарата, приготовленного по рецепту врача. Рекомендованная
ежедневная доза состава с немедленным
высвобождением, приготовленного по рецепту врача, составляет 40
миллиграмм в день, 10 мг в один прием. Состав с замедленным
высвобождением 4AP компании Акорда Терапьютикс
(Фампридин-СР) позволяет принимать дозу в 40 мг два раза в день.
Изначально применявшийся в качестве
репеллента от птиц, препарат 4AP
не является абсолютно безопасным и может иметь значительные побочные
действия. При этом достаточно сложно подобрать дозировку, дающую
максимальный эффект, но при этом приводящую к минимальным побочным
реакциям. В ряде случаев наиболее эффективная дозировка близка к
дозировке, вызывающей побочные действия. Поскольку 4AP
стимулирует нервную систему, побочные реакции включают в себя
бессонницу, нервозность, зуд, повышенное артериальное давление,
сердцебиение и судороги.
В опубликованном описании истории
болезни, потенциальная токсичность 4АР была зарегистрирована у
42-летнего мужчины с травмой на уровне С3, принимавшего 4 АР,
изготовленного по рецепту (4). Его таблетка 4АР содержала 10-кратную
дозировку, указанную на этикетке, т.е. дозу, которая обыкновенно
является токсичной. В результате он попал в реанимацию. Согласно
предоставленному отчету «у пациента наблюдается постоянная потеря
кратковременной памяти, после длительного и сложного стационарного
лечения».
Наблюдается определенное
расхождение точек зрения пациента и ученых на соотношение риска и пользы
при приеме 4AP. В частности многие
профессиональные статьи минимизируют риски, тогда как множественные
случаи, обсуждаемые на вебсайтах по ТСМ, свидетельствуют о том, что
зачастую эффект незначителен в сравнении с побочными эффектами.
Акорда Терапьютикс сыграла ведущую
роль в популяризации 4AP в качестве препарата,
восстанавливающего функции при ТСМ. К сожалению, через 10 лет этой
работы, компания перенаправила свои усилия на преимущества использования
4AP при рассеянном склерозе. В частности, в 2004
году компания закончила 3 двухфазных клинических исследования,
включающих в себя Фампридин-SR Возможно, из-за
ряда ограничивающих факторов, снизивших устойчивость к ошибкам,
результаты исследования не продемонстрировали достаточную статистическую
значимость для двух конечных пунктов исследования.
Далее обобщается ряд ключевых
исследований на людях в хронологическом порядке:
Dr. Robert Hansebout
1) Д-р Роберт Хансебаут
и др. (Канада) вводили 4AP восьми участникам
исследования с хронической ТСМ, в рамках рандомизированного
перекрестного исследования, в котором каждый пациент получал или плацебо
или 4AP, а затем меняли
лечение (5). Улучшение отмечалось в 5 из 6 случаев с неполной ТСМ; ни у
одного из пациентов с полной травмой прогресса не наблюдалось. Прогресс
включал в себя улучшение двигательного контроля и чувствительности, а
также сокращение спастичности и болей.
2) Dr.
Keith Hayes
2) Д-р Кейт Хайес
и коллеги (Канада) оценивали воздействие внутривенного введения 4AP
на электрофизиологическую проводимость у шести пациентов с ТСМ (6). У
двоих пациентов улучшилась проводимость по одному показателю
(соматосенсорные вызванные потенциалы), а у четырех улучшила
проводимость по другому показателю (моторные вызванные потенциалы).
Клинически сократилась спастичность (2 пациента), и боль (1 пациент),
улучшилась чувствительность (1), движение ног (3) и контроль дефекации
(1).
3) Dr.
Jack Segal
3)
Д-р Джек Сегал и др.
(США) продемонстрировали, что однократная 10-миллиграммовая доза 4AP
способствует улучшению легочной функции у пациентов с тетраплегией (7).
В частности, отмечалось увеличение жизненной емкости, максимального
давления при вдохе и выдохе через 6 часов после
применения, и в течение последующих 12 часов.
4)Dr. Patrick Potter
4) Д-р Патрик Поттер
и др. (Канада) описали прогресс трех пациентов с неполной квадриплегией,
принимавших дозы 4AP по 10 мг перорально два или
три раза в день в течение четырех месяцев (8). Помимо значительного и
длительного снижения спастичности, другие достижения включали в себя
снижение болевого синдрома (1 пациент), восстановление мышечной силы
(3), улучшение чувствительности (2), произвольный контроль дефекации
(1), эректильную функцию (2), улучшения функций кистей рук (1) и
улучшение способности передвигаться (2). Один пациент смог стоять с
поддержкой впервые за 16 лет после травмы.
5)Dr. Patrick Potter
5) Д-р Патрик Поттер
и др. доложили о результатах рандомизированного двойного слепого
перекрестного исследования, направленного на оценку безопасности и
эффективности Фампридина-SR, состава с
замедленным высвобождением 4AP (9). Двадцать
шесть пациентов с неполной ТСМ получали либо 4AP,
либо плацебо в течение двух недель, с последующим недельным периодом
вымывания, после которого группам меняли метод лечения. Положительный
эффект отмечался по показателям качества жизни, чувствительности,
движения, спастичности и удовлетворенности пациентов. Статистически
значимых достижений по таким показателям как болевой синдром, функции
мочеиспускания, дефекация, сексуальные функции, или функциональная
независимость зарегистрировано не было.
6) Dr. Jack Segal
6) Д-р Джек Сегал
и др. изучали воздействие 4AP на показатели
передвижения у девяти пациентов мужского пола (у шести – тетраплегия, у
трех – параплегия), сохранивших некоторую способность ходить (10). В эти
показатели входили скорость передвижения (метров в минуту), темп (шагов
в минуту), длина шага (метры), цикл ходьбы (секунды) и поддержка обеими
конечностями (процент цикла ходьбы). После приема 4AP были
отмечены статистически значимые изменения по ряду параметров
7) В рандомизированном исследовании
со слепыми дозировками, д-р Джек Сегал и др. сравнили
чувствительность и моторные функции 16 пациентов, получающих 4AP
по 30 мг в день (высокая доза) в течение 3 месяцев с пятью пациентами,
получавшими по 6 мг в день (низкая дозировка) (11). У пациентов,
получавших высокую дозу, снизилась спастичность, улучшились показатели
по моторике и чувствительности, а также функция легких.
8) В рандомизированном, двойном
слепом, перекрестном исследовании д-р Моник ван дер Брюгген и др.
(Нидерланды), пришли к заключению, что 4AP не оказывает статистически
значимого воздействия на функциональный статус, скорость ходьбы и
восприятие вибраций у 20 пациентов с неполной ТСМ (8).
9) Д-р Джек Сегал и др.
сравнили воздействие однократного применения 10 мг 4AP на вариабельность
частоты сердечных сокращений, в качестве показателя автономной нервной
системы, у 13 пациентов с ТСМ с 13 здоровыми пациентами контрольной
группы (13). Разница в показателях вариабельности частоты сердечных
сокращения в предварительном тесте у пациентов с ТСМ и пациентов
контрольной группы исчезла через 24 часа после применения 4AP.
10) Д-р Израэль Грихалва и
коллеги (Мехико) рандомизировали 27 пациентов для назначения либо
плацебо, либо растущих доз 4AP, принимавшихся в течение 12 недель, после
чего методы лечения менялись на противоположные. В сравнении с
контрольной группой плацебо, у пациентов, получавших 4AP, наблюдались
улучшения двигательной функции, чувствительности и самостоятельности.
Исследователи отметили длительное воздействие на чувствительность и
самостоятельность через 12 недель после того, как пациенты были
переведены в группу плацебо. У 55% пациентов
наблюдались побочные реакции.
11) Д-р Кейт Хайес и коллеги
изучили фармакокинетику у 16 пациентов с неполной ТСМ (группы B-D
по шкале ASIA) после применения 25-60 мг
фампридина- SR дважды в день в течение недели.
Пиковая концентрация в плазме крови наблюдалась 2,2-3,0 часа после
приема и период полувыведения длился 5,7-6,9 часов. Исследователи пришли
к выводу, что 1) побочные эффекты были слабо или умеренно выраженными и
не связанными с дозировкой, и 2) состав с замедленным высвобождением
медленно абсорбируется и выводится.
12) Компания «Акорда
Терапьютикс» спонсировала 2-фазовое клиническое исследование,
направленное на сравнение пациентов, принимающих высокую или низкую дозу
состава с замедленным высвобождением 4AP (т.е.
фампридина-SR) с группой, получающей плацебо
(16). В каждой группе было около 30 пациентов. У пациентов были неполные
травмы спинного мозга, полученные не менее 18 мес. назад (т.е.
хронические), в возрасте от 18 до 70 лет, на уровнях от С4 до Т10.
Восемьдесят процентов – мужчины, 92% - представители белой европеоидной
расы.
Пациенты получали по 40 мг
препарата и по 25 мг дважды в день в течение 4 недель. Сорок три
процента пациентов, принимавших высокие дозы препарата, вышли из
исследования в основном из-за различных побочных эффектов. Пациенты,
принимавшие низкие дозы, переносили препарат лучше, уровень отсева
составил всего 13%, что сравнимо с 10% отсева в группе плацебо.
Исходы оценивались по ряду
показателей, включая дневники-анкеты пациентов, оценку качества жизни,
эректильную функцию, контроль дефекации и мочеиспускания, спастичность и
клинические обзоры общего состояния. Хотя исследованию недостает
статистической значимости для твердых выводов по большому количеству
переменных показателей исходов, некоторые улучшения в качестве жизни,
спастичности и эректильной функции все же произошли.
13) Dr. Jack Segal
13) Д-р Джек Сегал и коллеги
(США) оценили воздействие 4АР на толерантность к глюкозе у 31 пациента с
травмами, полученными не менее 1 года назад (17). В целом, пациенты с
ТСМ склонны к нарушению толерантности к глюкозе, или диабету. Участники
исследования получали 75 грамм глюкозы натощак и затем проходили
пятичасовой тест на толерантность к глюкозе, который позволяет оценить
эффективность усвоения глюкозы из крови. На начало лечения у 29
пациентов из 31 отмечалось нарушение толерантности к глюкозе. Через 6
месяцев после перорального приема 4АР с немедленным высвобождением,
только у 12 отмечалось нарушение толерантности к глюкозе.
14) Dr.
Israel Grijalva
14)
Д-р Израэль Грихалва
и коллеги (Мехико) оценили
воздействие 4АР на опорожнение желудка у пациентов с хроническими
травмами (18). ТСМ отрицательно влияет на желудочно-кишечный тракт,
замедляя движение твердой пищи по желудку и кишечнику. Признаки
нейрогенного кишечника включают в себя уплотнение стула, запоры, вздутие
живота, длительную гигиену кишечника и длительный транзит по толстому
кишечнику. По оценкам специалистов 41-86% пациентов с ТСМ страдают от
хотя бы одной из этих проблем, и 41% посвящают гигиене кишечника, по
крайней мере, 1 час в день.
В
этом исследовании 18 пациентов с хронической ТСМ (9 - с шейным уровнем,
и 9 - с грудным) перорально получали 4АР в течение 12 недель ежедневно.
Оценивалось желудочно-кишечное опорожнение до и после периода лечения.
Результаты показали, что "прием 4АР значительно замедляет опорожнение
желудка у пациентов с хронической травмой спинного мозга, не зависимо от
уровня и группы по шкале ASIA".
2)
HP-184
Как и обсуждаемый ранее препарат
4AP, HP-184 усиливает
проводимость неповрежденных, но демиелинизированных аксонов, которые при
большинстве травм сохраняются в месте повреждения. Будучи усилителем
проводимости, это вещество не является лечением с позиций перманентной
регенерации нейронов, восстанавливающей функции, это лишь стимулятор уже
существующих нейронов, и восстановленные функции пропадают, как только
препарат метаболизируется и выводится из организма.
Проводимость зависит от
последовательного потока различных ионов (заряженных растворенных
молекул) внутрь и наружу из ионов, процесса, который нарушается, если
нейрон теряет свою изолирующую миелиновую оболочку. HP-184
блокирует каналы ионов, ингибирующих проводимость после потери миелина,
в результате травмы.
Компания Санофи-Авентис
Фармасьютикалс спонсировала несколько двухфазных (т.е. промежуточных)
клинических исследований, направленных на оценку безопасности и
эффективности HP-184. Последнее двойное слепое
мультицентровое исследование было начато в 2004 году с планируемым
включением 240 пациентов с неполной травмой спинного мозга группы
C-D по шкале ASIA,
полученной не раннее, чем за 18 месяцев до включения в исследования
(т.е. хронические травмы) (19). Уровень повреждений участников должен
находиться между шейным уровнем С4 и грудным Т10.
Хотя сведения о результатах пока
практически отсутствуют, некоторые участники рассказали о своем опыте в
индивидуальном порядке. Например, через шесть месяцев лечения, один
пациент подтвердил, что восстановил чувствительность по всему телу и в
значительной степени мышечную силу. В другом случае женщина сообщила,
что «смогла самостоятельно уверенно стоять, начала тренировать подъем по
ступенькам, все активизировалось». Побочные реакции включали в себя
головные боли, тошноту и утомляемость. Как и предполагалось, все
достигнутые улучшения пропали после отмены препарата.
3)
THEOPHYLLINE STIMULATION OF RESPIRATION
3) СТИМУЛЯЦИЯ ДЫХАНИЯ
ТЕОФИЛЛИНОМ
Существуют факты, свидетельствующие
о том, что теофиллин стимулирует дыхание у пациентов с угнетенной в
результате шейной ТСМ дыхательной функцией. Теофиллин, расслабляющий
гладкую мускулатуру бронхов, десятилетиями использовался для лечения
астмы и бронхита. В результате накоплено значительное количество
клинических данных, подтверждающих безопасность его применения.
Движущей силой изучения потенциала
теофиллина в качестве усилителя дыхательной функции при ТСМ выступил д-р
Гарри Гошгарян (США). Ученые под его руководством выполнили
множество исследований на животных, которые позволили определить то,
каким образом теофиллин оказывает свое воздействие, и инициировали
исследование на людях.
Теофиллин найден в кофе и чае, и
близко родствен кофеину. При метаболизме кофеина и потери специфической
метиловой группы, формируется теофиллин. Теофиллин также схож по
структуре с аденином, одним из пуриновых оснований в нашей ДНК, и с
пуриновым основанием обоих АТФ (аденозинтрифосфатов), переносчиком
повсеместной энергии, и цАМФ (циклический аденозинмотофосфат),
посредником в важных клеточных и нейрональных процессах.
Теофиллин блокирует рецепторы
аденозина, ингибирующие дыхательную деятельность (т.е. является
антагонистом). Как ключ, который входит в замочную скважину, но не может
повернуться и открыть замок, теофиллин достаточно схож по структуре с
аденином, чтобы заблокировать доступ к рецепторам, но при этом имеет
достаточное количество отличий для того, чтобы не активировать
рецепторы. Теофиллин блокирует энзим, разлагающий цАМФ, что приводит к
увеличению внутриклеточного цАМФ. Исследования на животных показали, что
увеличение уровней цАМФ способствует преодолению ингибиторов роста
центральной нервной системы растущими аксонами и увеличивает их
проводимость.
Теофиллин активирует
перекрестный дифрагмальный путь, обычно находящийся в спящем
состоянии, запасной путь, который, по-видимому, отчасти восстанавливает
диафрагмальную функцию после ТСМ (20-22). Поскольку этот путь находится
в другой части спинного мозга, чем первичный респираторный путь, травма,
повреждающая первичный путь, может пощадить запасной путь. Как правило,
дополнительный путь неактивен, т.е. несмотря на наличие неповрежденных
нейрональных связей между мозгом и диафрагмой, импульсы по нему не
передаются.
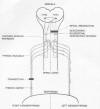
Нервные импульсы, сокращающие
диафрагму, исходят из нервных клеток головного мозга. Эти нейроны
соединяются с нейронами (диафрагмальные ядерные нейроны), расположенными
по сторонам шейного отдела спинного мозга С3-5. В свою очередь, эти
нейроны передают сократительные импульсы к диафрагме.
Некоторые нейроны, исходящие из
головного мозга, расщепляются и пересекают другую сторону спинного мозга
до соединения с нейронами диафрагмы. Следовательно, даже если травма
может нарушить основной нервный путь, эти пересекающие нервы не будут
затронуты, обеспечивая прямую, хотя и неактивную, связь от головного
мозга к парализованной диафрагме. Теофиллин значительно стимулирует
обычно спящий перекрестный диафрагмальный путь, и позволяет
импульсам, восстанавливающим функцию, достичь диафрагмы.
В исследованиях на животных
Гошгарян и коллеги продемонстрировали, что восстановление при помощи
теофиллина продолжалось в течение 30 дней после прекращения приема
препарата. Соответственно, Гошгарян пришел к выводу, что постоянные
улучшения дыхательной функции после прекращения приема препарата были
вызваны нейрональной пластичностью (т.е. способностью адаптироваться),
индуцированной теофиллином, а не только блокированием аденозиновых
рецепторов.
Коллектив Гошгаряна изучил
воздействие теофиллина на пациентов с шейной травмой:
1) Пациент с ассиметричной С5-7
травмой 20-летней давности получал теофиллин внутривенно в стационаре на
стадии изучения непосредственных эффектов препарата, и перорально в
течение нескольких недель дома. Гошгарян сообщает: «… в ходе обеих
стадий исследования было отмечено значительное улучшение респираторной
мышечной функции у пациента на 172%. Общая мышечная сила на вдохе …
увеличилась на 25% на стадии перорального приема».
«Более того, согласно другому
тесту, косвенно замеряющему степень дыхательных импульсов, идущих от
головного мозга к спинному (нисходящая активность дыхательного центра),
у пациента были отмечены улучшения во время обеих стадий исследования,
во время поверхностного и глубокого дыхания, на 20-171% после назначения
препарата».
2) В сравнительно недавнем случае,
мужчина, получивший шейную травму 30 лет назад в результате
огнестрельного выстрела, был снят с искусственной вентиляции легких
после лечения теофиллином. У пациента была травма с правой стороны
спинного мозга на уровне С5, и с левой стороны – на уровне С6. Он
поступил в стационар из-за респираторной недостаточности, вызванной
бактериальной пневмонией и сепсисом. Хотя инфекции были успешно
вылечены, ему по-прежнему требовалась искусственная вентиляция легких,
до лечения теофиллином месяц спустя. После внутривенного введения
теофиллина в течение дня, различные дыхательные показатели улучшились, и
пациент был снят с искусственной вентиляции в тот же день.
3) В двойном слепом,
плацебо-контролируемом, перекрестном исследовании Гошгарян и коллеги
пролечили теофиллином 10 пациентов с шейной ТСМ (24). Хотя общие
результаты не показали значительной разницы между плацебо и теофиллином,
у 40% участников наблюдался выраженный прогресс по респираторным
показателям. Степень повреждения, по-видимому, более важна при
прогнозировании полезного воздействия теофиллина, чем уровень травмы.
4)
Lithium
4) Литий
Д-ра Ят-ва Вонг и Уайз Янг
и коллеги создали сеть китайских центров по
ТСМ для выполнения клинических исследований по перспективным методам
лечения. Начальные исследования сети будут посвящены изучению применения
лития и стволовых клеток, полученных из пуповинной крови. Эти два
подхода рассматриваются вместе, так как предварительно полученные факты
позволяют предположить, что литий стимулирует пролиферацию данных клеток
и выделение полезных факторов роста нейронов.
Элемент с низким молекулярным
весом, используемый в качестве медицинского препарата для лечения
биполярного расстройства или депрессии при маниакально-депрессивном
психозе, литий оказывает значительное воздействие на нервную систему
посредством ряда действенных физиологических механизмов. Поскольку
терапевтические дозировки лишь незначительно ниже дозировок, считающихся
токсичными, была инициирована предварительная первая стадия исследования
для изучения безопасности и фармакокинетики лития (т.е. абсорбции,
распределения, выведения и т.д.) на 20 пациентах с полной или с неполной
травмой (группы A-C по шкале ASIA), получивших травмы не менее года
назад (т.е. хронические травмы). Участники исследования получали литий
примерно в таких же дозах перорально, как и для лечения депрессии при
маниакально-депрессивном психозе. В течение 6 недель было
зарегистрировано 95 побочных эффектов, в основном желудочно-кишечных
расстройств или тошноты, и, в результате, семеро участников вышли из
исследования. Янг пришел к заключению, что "препарат безопасен и не
приводит к каким-либо значительным побочным действиям".
В 2009 году группа исследователей
завершила более крупное исследование 2 фазы, где 40 участников с
хронической ТСМ рандомизированно принимали либо литий, либо плацебо в
течение 6 недель. В отличие от предыдущего исследования только двое
участников вышли из исследования. Интересно отметить, что участники,
принимавшие литий меньше страдали от нейропатических болей, часто
встречающейся проблемы пациентов с ТСМ. Снижение болей длилось еще в
течение 6 месяцев после окончания исследования.
В качестве последовательного
продолжения этих исследований, было начато исследование 2 фазы,
направленное на оценку имплантации выше и ниже повреждения спинного
мозга пациентам с хронической ТСМ растущего количества стволовых клеток,
полученных из пуповинной крови, в комбинации с лечением литием. Затем, в
исследовании 3 фазы ученые планируют произвести имплантацию стволовых
клеток 400 пациентам, рандомизированным по группам приема плацебо или
лития в течение 6 недель. Центры в США планируют провести аналогичные
исследования.
Подобный акцент на литии
объясняется результатами ряда многообещающих исследований на животных.
Сначала, д-р Л.В. Йик и коллеги (Гонконг) пролечили крыс с
экспериментальной травмой литием и ферментом, именуемым хондроитиназой,
который перерабатывает ключевой молекулярный компонент рубца на месте
повреждения, ингибирующего регенерацию аксонов (30). У пролеченных крыс
наблюдалась более выраженная регенерация аксонов и движение передних
конечностей. Второе исследование проведено д-ром Х.Су и др.
(Гонконг), где было продемонстрировано, что клинически релевантные дозы
лития усиливают пролиферацию нейральных прогениторных клеток,
пересаженным крысам в спинной мозг, и снижали посттравматический
иммунный отклик, снижающий регенерацию (31-32). А также, д-р Ф.Форнай
и коллеги (Италия) продемонстрировали, что литий задерживает
прогрессирование такого нейродегенеративного заболевания как боковой
амиотрофический склероз (БАС) у людей, а также на моделях этого
заболевания у мышей (33).
5)
Fibroblast
Growth
Factor
(FGF)
5) Фактор роста фибробластов
(ФРФ)
Д-р Генрих Ченг
и коллеги (Тайвань) пролечили девять пациентов с хроническими шейными
травмами фактором роста фибробластов (34). Множественные исследования на
животных позволяют предположить, что ФРФ способствует регенерации после
травмы, стимулируя реваскуляризацию места повреждения, выживаемость
поврежденных нейронов и рост аксонов. Из девяти пациентов 8 были
мужского пола, возраст варьировался от 25 до 63 (в среднем 48), и время
с получения травмы колебалось от 5 месяцев до 8, 5 лет (в среднем 2,6).
Шесть пациентов получили травму в мотоциклетной аварии, двое при
падении, один при огнестрельном ранении.
Спинной мозг каждого пациента был
подвергнут цервикальной ламинэктомии, и внешняя оболочка спинного мозга
была рассечена. При необходимости, проводилась декомпрессия спинного
мозга, и спинной мозг был освобожден от сдавливающих рубцовых тканей.
ФГФ в матриксе из фибринового клея был наложен на спинной мозг, позволяя
этому фактору роста, питающему нейроны, медленно проникнуть в место
повреждения.
Функциональный статус пациентов
оценивался до операции, и каждый месяц после, в течение полугода. Оценка
включала в себя повседневную деятельность, функциональные способности,
спастику, силу движений, чувствительность и боль. По шкале от 1 до 100,
моторные показатели улучшились от 52 до 69, болевая чувствительность от
61 до 72, и поверхностная чувствительность от 57 до 72. У некоторых
пациентов улучшился контроль мочеиспускания и дефекации, и снизилась
боль. Одни пациент перешел из группы А (полная травма) по шкале ASIA в
группу С (неполная травма), другой – из группы С в группу D, т.е.
улучшение функции. Восемь пациентов продемонстрировали прогресс
неврологического уровня повреждения, например, один пациент, с
сохраненными функциями от уровня С5 прогрессировал до уровня Т1. Ученые
пришли к выводу: «Умеренная регенерация нервов произошла у 9 пациентов
после данной процедуры без каких-либо побочных реакций».
Хотя ученые отмечают определенные
ограничения данной предварительной фазы исследования, тем не менее, они
считают, что результаты оправдывают дальнейшие более глубокие
исследования. Принимая во внимание ограничения данного исследования,
сложно различить, вызваны ли умеренные улучшения лечением ФРФ
хирургической декомпрессией или удалением тканей или же агрессивной
реабилитацией после оперативного вмешательства.
TOP