CELL TRANSPLANTATION
Эта область в настоящее время
быстро развивается и является одним из наиболее перспективных обещаний
будущего. В связи с этим, некоторый материал устаревает довольно быстро,
но, тем не менее, предоставляет читателю практический обзор различных
программ клеточной трансплантации, появляющихся в мире. Размер раздела
не свидетельствует о значимости материала, а лишь отражает авторский
подход к информации. Список программ не является всеохватывающим.
Несомненно, некоторые из процедур
относительно безобидны, а некоторые предполагают значительный риск.
Соответственно, каждый, кто думает о проведении той или иной процедуры,
должен тщательно взвесить потенциальную пользу и оценить возможный
риск, как правило, не слишком четко определенный, применительно к своему
конкретному случаю и с позиции собственных приоритетов. Многие из этих
программ были изначально разработаны исключительно из альтруистических
побуждений, тогда как некоторые имеют экономические стимулы, что
характерно практически для всех биотехнологических и фармацевтических
компаний. Однако подобная экономическая мотивация не обязательно носит
отрицательный характер, если мы действительно хотим увидеть методы
лечения ТСМ сегодня вне научно-академической среды. Тем не менее,
caveat emptor!!*
Introduction
Введение
Прежде чем начать обсуждение
отдельных процедур трансплантации, необходимо представить краткий обзор
различных типов клеток и процедур, входящих в программы клеточной
трансплантации, которые направлены на восстановление ряда функций после
ТСМ. Читателям, желающим получить, более подробную информацию, можно
порекомендовать следующие книги: Stem Cell Now
(«Стволовые клетки сейчас») и Human Embryonic Stem Cells
(«Эмбриональные стволовые клетки человека»).
Olfactory Tissue/Cells
Обонятельная ткань/клетки:
Поскольку обонятельная ткань подвергается воздействию воздуха, которым
мы дышим, она содержит клетки, обладающие значительным потенциалом к
обновлению, включая обновляемые нейроны, прогениторные стволовые клетки
и клетки обонятельной выстилки (КОВ). Уникальная природа этой ткани и ее
потенциал, катализирующий регенерацию, в настоящее время изучается в
свете использования для лечения различных неврологических заболеваний
помимо ТСМ, а именно, таких как болезнь Паркинсона и боковой
амиотрофический склероз.
При трансплантации в поврежденный
спинной мозг, КОВ потенциально стимулируют регенерацию аксонов секрецией
изолирующих миелиновых оболочек вокруг растущих и поврежденных аксонов,
выделяя факторы роста, а также структурные и матричные макромолекулы,
которые прокладывают путь для растущих аксонов.
Stem Cells
Стволовые клетки:
Вкратце, стволовые клетки это клетки-предшественники, или прогениторные
клетки, которые обладают способностью трансформироваться в широкий
спектр тканей. Хотя, как правило, их дихотомически подразделяют либо на
эмбриональные клетки, либо взрослые, они на самом деле, представляют
собой континуум типов клеток, который может трансформироваться в
конечный продукт – ткань.
Например, по мере развития нашей
центральной нервной системы (ЦНС), эмбриональные стволовые клетки
развиваются в более специализированные тканеспецифичные нейральные
стволовые клетки. В свою очередь, эти тканеспецифичные клетки могут
дифференцироваться на нейронально или глиально рестриктированные
клетки-предшественники, при этом первые обладают потенциалом
трансформироваться в нейроны, а последние – в клетки, именуемые
олигодендроцитами и астроцитами.
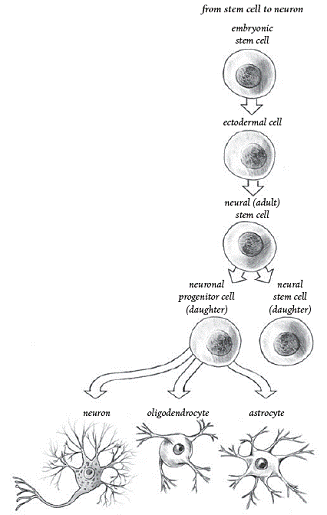
Омнипотентные эмбриональные клетки
обладают наибольшей способностью дифференцироваться на широкий спектр
клеточных типов, хотя задать нужное направление их дифференциации
довольно сложно. Взрослые стволовые клетки находятся в большинстве
тканей, включая, например, ЦНС, костный мозг, кожу, тонкий кишечник,
печень, мышцы, волосяные луковицы, и даже зубы. Иногда их экспрессия
интенсивна, как например, постоянное пополнение запасов клеток крови
костным мозгом; в других тканях они неактивны и нуждаются в
дополнительном воздействии для активации.
Хотя взрослые стволовые клетки
обычно дифференцируются на специализированные клетки, связанные с
первичной тканью, при наличии определенных сигналов, они также могут
трансформироваться в клетки других тканей. Например, при определенных
обстоятельствах, стволовые клетки костного мозга могут
дифференцироваться на нервные клетки, и, действительно используются в
ряде трансплантационных программ при ТСМ. Более того, исследования
свидетельствуют о том, что взрослые стволовые клетки могут быть
перепрограммированы обратно, в более эмбриональное состояние. Помимо
всего вышесказанного, хотя мы и выделили терапевтический потенциал
стволовых клеток, при получении неправильных сигналов, клетки могут
стать и причиной физиологических нарушений, в частности, вызывая,
например, рак.
Embryonic Stem Cell (ESC) Isolation
Изоляция эмбриональных стволовых
клеток (ЭСК): После оплодотворения яйца,
формируется эмбрион, который затем делится на двухклеточный эмбрион. В
книге «Стволовые клетки сейчас», автор Кристофер Скотт сравнивает
процесс деления с разделением ножом мыльного пузыря, тем самым, создавая
два меньших пузыря с общим объемом в пределах первого. Разрезав еще раз,
мы получаем четыре пузыря, или четырехклеточный эмбрион. Это деление
продолжается, успешно создавая 8, 16, 32, 64, 128-клеточный эмбрион, при
этом общий объем сохраняется прежним.
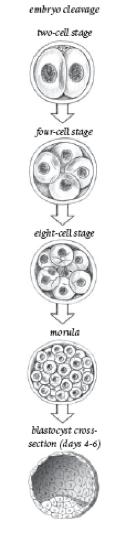
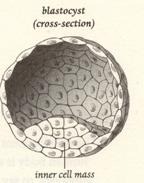
С четвертого по шестой день, клетки
выстраиваются в два ряда: внешний слой, который разовьется в
плацентарную и амниотическую ткани, и еще несколько десятков клеток,
так называемую внутреннюю клеточную массу (ВКМ), которая в будущем
превратится во все остальное. Теперь эмбрион, именуемый бластоцистой,
имеет примерно 0.1-мм в поперечнике, или размер с точку в конце этого
предложения.
По мере того, как клетки делятся,
они все больше теряют свои омнипотентные свойства. Примерно через две
недели, клетки ВКМ начинают выстраиваться в три особых слоя, которые
становятся различными тканями:1) эктодермальный слой (развивается в
нервы, кожу и т.д.), 2) мезодермальный слой (становится кровью, мышцами,
костями и т. д.), и 3) эндодермальный (дифференцируется на кишечник,
печень, поджелудочную железу, мочевой пузырь и т.д.).
Чтобы получить ЭСК, клетки ВКМ
изолируются до того, как они начнут превращаться в эти новые слои, и
выращиваются в культуре. Технология культивирования появилась совсем
недавно и требует очень сложной методологии и умений. Например, чтобы
обеспечить клеткам питательные вещества и специальную систему сигналов,
чтобы избежать дальнейшей дифференциации, ученым приходилось их
выращивать на слое клеток животных.
Schwann Cells
Шванновские клетки:
Эти клетки ответственны за ремиелинизацию аксонов периферической нервной
системе, которой, в отличие от ЦНС, обладает значительным регенеративным
потенциалом. В течение многих лет ученые пытались использовать потенциал
этих клеток для того, чтобы воспроизвести аналогичное регенеративное
воздействие при введении в поврежденный спинной мозг.
Cell Source
Источник клеток:
Клетки, пригодные для трансплантации, можно получить у самого пациента
(аутологичные); у генетически отличных индивидуумов, эмбрионов, или из
пуповинной крови (аллогенные); или у других видов (ксеногенные). Все три
типа использовались для трансплантации в попытке восстановить функцию
после ТСМ. Поскольку аутологичная ткань взята у самого пациента,
иммунное отторжение отсутствует. Недифференцированная природа
эмбриональных, и, в меньшей степени, клеток пуповинной крови, также
минимизирует отторжение. В целом клетки отбираются исходя из легкости их
изолирования, как например, концентрированные клетки крови, а, не
основываясь на их регенеративном потенциале или теоретически оптимальном
источнике.
Site of Transplantation
Место трансплантации:
Донорские клетки пересаживаются пациенту различными методами, включая
введение в спинной мозг или спинномозговую жидкость, внутривенное
введение, или внутримышечное. Конечно, проще и безопасней ввести клетки
в мышцы, кровь или спинномозговую жидкость, чем добираться до спинного
мозга хирургическим способом, что, однако, может быть и не так
эффективно. Остается множество неясных деталей, например, достигают ли
клетки, трансплантированные этими разнообразными способами, места
повреждения и оказывают ли они какое-либо положительное воздействие.
Хотя необходимо еще большее количество исследований, ученые начали
изучать судьбу трансплантированных клеток на моделях ТСМ у животных.
Например, чешские ученые
разрабатывают процедуры с использованием магнитно-резонансной
томографии. Кратко, суть заключается в следующем: очень маленькие
магнитные частицы оксида железа прикрепляются к стволовым клеткам,
которые таким образом становятся видимыми на МРТ, и появляется
возможность проследить за ними после трансплантации. Общая цель
исследования заключается в определении времени миграции к месту
повреждения и срока, в течение которого клетки там находятся. Подобная
информация помогает нам определить оптимальные сроки для трансплантации,
необходимое количество клеток и оптимальный способ введения.
Или же другой пример: международная
команда ученых использовала магнитно-резонансные методы исследования для
оценки миграции клеток обонятельной выстилки носа, помеченных оксидом
железа, которые вводились крысам в спинной мозг. Маркированные КОВ можно
наблюдать в спинном мозге, по крайней мере, в течение двух месяцев после
трансплантации. Хотя в здоровом спинном мозге наблюдалась экстенсивная
миграция трансплантированных клеток в обоих направлениях, клетки
оказались неспособны пересечь рубец в поврежденном спинном мозге.
Age & Level of Injury
Возраст и уровень травмы:
На эффективность лечения стволовыми клетками могут влиять и другие
факторы, включая и возраст, и уровень травмы. Как продемонстрировали
британские ученые, именно это и происходит в случае использования
стволовых клеток костного мозга, которые трансплантируются в ряде
программ по лечению ТСМ. В этом исследовании костный мозг был изолирован
из подвздошного гребня (т.е. области таза) доноров с ТСМ и
прокультивирован. Возраст доноров варьировался от 23 до 66 лет, у всех
была полная травма, полученная в период от 5 месяцев до 23 лет на момент
забора костного мозга. Несмотря на ограниченный размер образца, рост
стволовых клеток в культуре был выше, если клетки были забраны у более
молодых пациентов, и у пациентов с шейным уровнем травмы.
Д-р Карлос Лима, занимающийся
трансплантацией обонятельной ткани, содержащей стволовые клетки, не
принимает пациентов старше 40 лет из-за снижения регенеративного
потенциала этой ткани с возрастом.
TOP